 |
|---|
| 特別寄稿 不溶化にもっと科学を |
|||
 |
九州大学教授 大学院農学研究院 植物資源科学部門 和田 信一郎 |
|
|
1.重金属類の不溶化技術の重要性 2.不溶化機構が十分明らかな処理法 |
| 酸化物鉱物や水酸化物鉱物は、その結晶の内部構造にかかわらず、表面はびっしりとヒドロキシ基(-OH)で覆われています。表面のヒドロキシ基はかなり反応性が高く、たとえば鉛イオンやヒ酸イオンと次のように反応します。この反応は表面錯形成反応と呼ばれています。 つまり、表面錯形成反応は吸着反応の一種ではありますが、重金属類と表面との間にはかなり強い化学結合が形成されているのです。 実は、土にはほとんど普遍的に含まれる酸化鉄鉱物の表面にも同じようにヒドロキシ基が存在するので、不溶化剤として機能します。図2は、3種の土に硝酸鉛溶液を添加し、水酸化ナトリウムを加えてpHを調節しながら、溶液中の鉛濃度を測定したものです。pHを上昇させると鉛濃度がどんどん低下しています。土によって異なりますが、あるpH以上では溶出量基準以下になっています。これは鉛イオンが、土に含まれる鉱物の表面のヒドロキシ基によって図1のような反応に従って固定されたものです。 pHを上昇させたとき鉛濃度が低下するのは、水酸化鉛の沈殿が生ずるせいもあるのではないかと考える方もいるかもしれませんが、それは違います。図2に示した折れ線は水酸化鉛の溶解度を示す線です。鉛が単に水酸化鉛として沈澱しているだけなら、この線が示す濃度以下にはなりません。 しかも、土によってはpH調節後、時間が経つにつれ鉛濃度はさらに低下します。これは鉛が鉱物の内部に入っていくためだと考えられています。図3はある土に含まれる水酸化鉄鉱物粒子の一部の電子顕微鏡写真です。黒い縞として映っているのは鉱物の結晶格子ですが、微結晶の端から端まで伸びておらず途中で途切れています。このように、土の鉱物には欠陥部が多く、いったん表面に結合した鉛イオンなどがこのような欠陥部に沿って内部に移動すると考えられています。 |
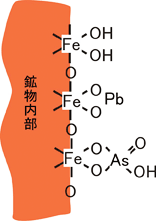 図1.水酸化鉄鉱物上の鉛イオンとヒ酸の表面錯体 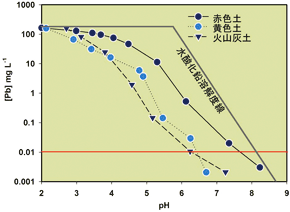 図2.土のpH調節による鉛の不溶化  図3.土の水酸化鉄鉱物の結晶格子の 電子顕微鏡写真 |
| 4.さらなる研究が必要なことがら 不溶化処理の適用を検討している方々が一番知りたいことは、処理土の安定性でしょう。1年程度の期間内での安定性であれば、少し頑張って処理土のモニタリングを継続すれば評価することができます。しかし、10年とか100年となるとそうはいきません。処理によって重金属類が、どのような形態に転換されるのかを特定することが重要になります。ところが、このような立場からの研究はまだ不十分です。 たとえば、ヒ素汚染土に鉄塩を添加するとヒ素はヒ酸鉄として固定されると考えられがちですが、そうとは限りません。なぜなら、鉄は水酸化物を形成しやすく、濃度によっては土に添加する鉄塩水溶液の中にすでに水酸化物鉱物が生成することもあります。また土に添加されると、ヒ酸と反応する前に土と反応して水酸化物鉱物になることもあります。このような場合、ヒ素はヒ酸鉄ではなく、図1のような表面錯体となっている可能性の方が高くなります。 また、最近マグネシア(酸化マグネシウム)系の不溶化資材が注目されています。これは鉛、ヒ素、セレン、シアン、フッ素など多くの重金属類の不溶化に効果があります。不溶化の効果は、溶出試験という明快な方法で確認されているので疑う余地はありません。しかしフッ素以外のものについては不溶化の機構は不明といってもいいくらいです。マグネシアはアルカリ性の資材ですから土に添加すると土の間隙水のpHは上昇します。すると、土に含まれる鉱物自体が、図2に示したように不溶化資材として機能します。マグネシア自体が重金属を固定しているのか、マグネシアのアルカリ性による間接的な効果なのかよく分かっていません。 |
| マグネシアは反応性の高い物質です。土に含まれる石英とさえ反応して新しい鉱物を生成したりします。図4はマグネシアと石英の反応によって石英表面に生成した微小鉱物の電子顕微鏡写真です。このような鉱物が生成し、その中に重金属類が取り込まれている可能性もあります。 安定性を科学的に議論するためには、不溶化処理研究にもっと科学が必要と思われます。放射性廃棄物の地層処分における人工バリアの研究と同じような考え方で進める必要があるのではないでしょうか。 |
 図4.マグネシアと反応させた石英表面に 図4.マグネシアと反応させた石英表面に生成した鉱物 |
 |
|---|